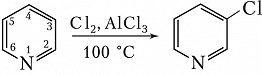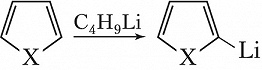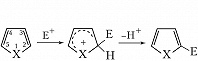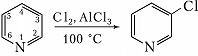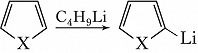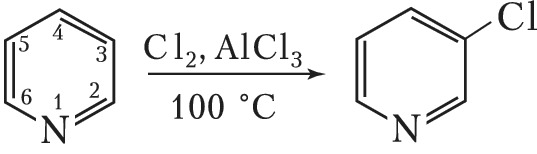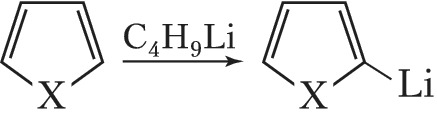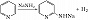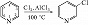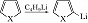ГЕТЕРОЦИКЛИ́ЧЕСКИЕ СОЕДИНЕ́НИЯ
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
ГЕТЕРОЦИКЛИ́ЧЕСКИЕ СОЕДИНЕ́НИЯ (гетероциклы) (от гетеро… и греч. ϰύϰλος – круг, цикл), органич. соединения, молекулы которых содержат циклы, включающие наряду с атомами углерода один или неск. атомов др. элементов (гетероатомов). Наибольшее значение имеют Г. с., содержащие гетероатомы N, O, S; менее изучены Г. с. с гетероатомами P, B, Sn, Si и др. Названия Г. с. дают в соответствии с правилами химич. номенклатуры. Важнейшие Г. с. имеют тривиальные названия, напр. акридин, индол, пурин. Г. с. отличаются друг от друга числом атомов в цикле: содержащие 3–4 атома относят к малым гетероциклам (напр., этиленоксид, оксетан), содержащие 5–10 атомов – к средним гетероциклам (фуран, пиразин, азепин и др.), содержащие более 11 атомов (напр., краун-эфиры, порфирины) – к макрогетероциклич. соединениям; наиболее устойчивые и распространённые – пяти- и шестичленные гетероциклы. Г. с. отличаются также числом гетероатомов в цикле; напр., среди пятичленных азотсодержащих Г. с. выделяют: пиррол – с одним атомом азота, пиразол и имидазол – с двумя (различаются взаимным расположением атомов азота в цикле), триазолы – с тремя, тетразол – с четырьмя атомами азота. В предельном случае, когда цикл состоит только из гетероатомов, образуются неорганические циклич. соединения (боразол, циклические фосфазены и др.). Г. с. характеризуются наличием заместителей, мостиковых или конденсиров. систем, а также насыщенным, ненасыщенным или ароматич. характером гетероцикла.
Г. с., удовлетворяющие критериям ароматичности, называют гетероароматич. соединениями. Среди них выделяют: π-избыточные – пятичленные Г. с. с одним гетероатомом т. н. пиррольного типа, в которых секстет π-электронов распределён на пяти центрах, напр. пиррол, тиофен, фуран; π-дефицитные – шестичленные Г. с. с одним или несколькими гетероатомами т. н. пиридинового типа, в которых секстет π-электронов распределён, как и в молекуле бензола, на шести центрах, однако один или неск. центров обладают более высокой электроотрицательностью, чем атом углерода, вследствие чего система обедняется π-электронами, напр. пиридин, пиримидин; π-амфотерные, или азолы, – пятичленные Г. с. с несколькими гетероатомами, из которых по крайней мере один – атом N пиридинового типа, а другой – атом O, S или N пиррольного типа, напр. тиазол, оксазол.
Насыщенные Г. с. по химич. свойствам близки к соответствующим алифатич. соединениям; так, насыщенные гетероциклич. простые эфиры (напр., тетрагидрофуран) подобны алифатич. простым эфирам, гетероциклич. амины (пиперидин и др.) – алифатич. вторичным аминам, лактоны – сложным эфирам, лактамы – амидам кислот. Ненасыщенные Г. с., вследствие взаимного влияния двойной связи и гетероатома, а также отсутствия стабилизации за счёт сопряжения, менее стабильны и отличаются по свойствам от соответствующих алифатич. соединений. Гетероароматич. соединения отличаются от неароматических Г. с. более высокими показателями преломления и поглощением в близкой УФ или видимой области спектра. Для них характерны наличие т. н. кольцевого тока и сигналы в слабопольной («ароматической») части спектра ЯМР (6,5–8,0 м. д. для 1Н и 110–170 м. д. для 13С).
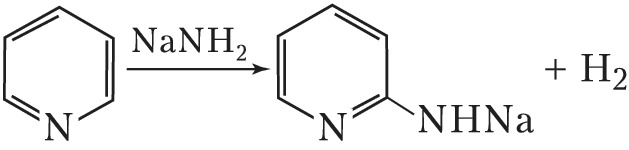
Гетероароматич. соединения вступают в типичные для ароматических соединений реакции замещения. Для π-дефицитных гетероароматич. соединений наиболее характерны реакции нуклеофильного замещения, напр.:
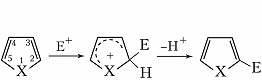
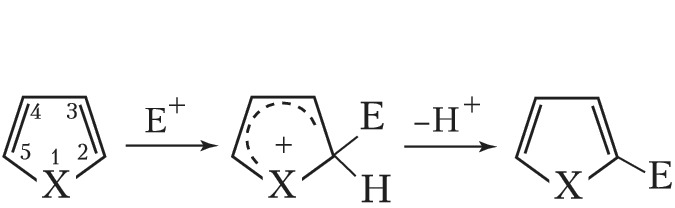
Для π-избыточных – реакции электрофильного замещения (галогенирование, нитрование, сульфирование, алкилирование и ацилирование) по механизму присоединения – отщепления в положение 2 молекулы:
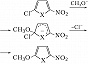
(X – NH, S, O; Е – электрофильный реагент). π-Дефицитные Г. с. вступают в реакции электрофильного замещения в жёстких условиях в положение 3 молекулы, напр.:
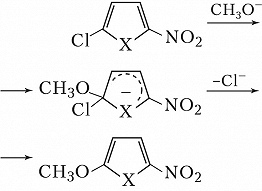
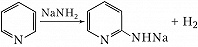
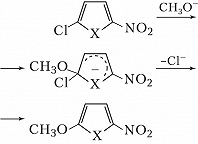
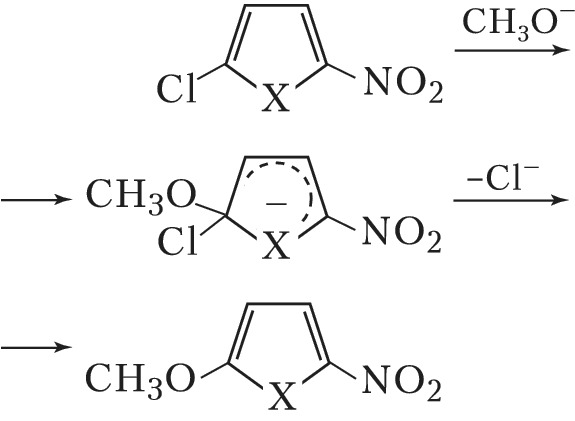
π-Избыточные гетероароматич. соединения вступают в реакции нуклеофильного замещения при наличии электроноакцепторного заместителя, напр.:
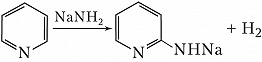
Для этих соединений характерны также реакции прямого металлирования, напр.:
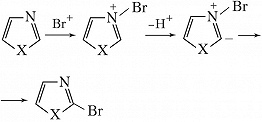
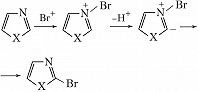
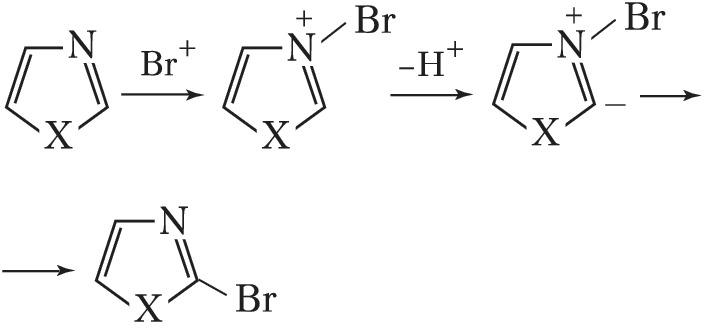
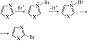
π-Амфотерные Г. с. по реакционной способности занимают промежуточное положение между π-дефицитными и π-избыточными гетероароматич. соединениями. Многие из них вступают в реакции электрофильного замещения по традиц. механизму присоединения – отщепления (1,2-азолы замещаются в положение 4; 1,3-азолы – в положение 5); в слабощелочной среде 1,3-азолы способны реагировать с электрофилами также по механизму т. н. илидного замещения, при этом в возникающем биполярном ионе (илиде) электрофил (напр., бром) направляется в положение 2:
Для гетероароматич. соединений характерны также реакции присоединения, напр. гидрирование (каталитическое или водородом в момент выделения), и обмена гетероатомами (напр., фуран в смеси с H2S или NH3 при 450 °С, катализатор Al2O3, превращается соответственно в тиофен или пиррол). Окисление гетероароматич. соединений происходит либо с раскрытием цикла, либо по гетероатому N или S с образованием N-оксидов или S,S-диоксидов.
Г. с. – самый многочисл. класс органич. соединений, включающий ок. 2/3 всех известных природных и синтетич. органич. веществ. К Г. с. относятся: большинство алкалоидов, мн. витамины, антибиотики (пенициллины и др.), пигменты (напр., хлорофилл, антоцианы); в виде структурных фрагментов Г. с. входят в молекулы белков и нуклеиновых кислот. Г. с., содержащие атомы азота и серы, выделяют из каменноугольной смолы и некоторых нефтей; производные фурана (гл. обр. фурфурол) получают гидролизом полисахаридов, содержащихся в отходах переработки с.-х. культур (напр., подсолнечника, кукурузы) и древесины. Многие Г. с. получают в пром-сти специфич. синтетич. методами, а также с помощью циклоприсоединения или внутримолекулярных перициклических реакций. Используют в произ-ве лекарственных препаратов, антибиотиков и витаминов, средств защиты растений, красителей, ВВ, полимерных материалов.