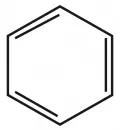
Бензол
Бензо́л, простейший представитель ароматических углеводородов, С6H6. Был открыт в 1825 г. М. Фарадеем, который выделил бензол из жидкого конденсата светильного газа; в чистом виде получен в 1833 г. Э. Митчерлихом пиролизом кальциевой соли бензойной кислоты. В 1865 г. Ф. А. Кекуле предложил формулу строения бензола с чередующимися простыми и двойными связями.
Бензол – бесцветная жидкость с нерезким запахом; tпл 5,53 °C, tкип 80,1 °C. Практически нерастворим в воде, смешивается во всех соотношениях с большинством неполярных органических растворителей; растворяет жиры, каучуки, смолы; с водой и спиртами образует азеотропные смеси. В молекуле бензола атомы углерода, находящиеся в состоянии sp2-гибридизации, образуют плоский, правильный шестиугольник с расстоянием между атомами углерода 139 пм, причём все атомы цикла участвуют в образовании единой π-электронной системы. Молекула бензола удовлетворяет всем критериям ароматичности.
Бензол обладает химическими свойствами ароматических соединений. При нитровании бензола смесью концентрированной HNO3 и H2SO4 образуется нитробензол, который может быть восстановлен в анилин. Бензол сульфируют концентрированной H2SO4 до бензолсульфокислот; алкилируют алкилгалогенидами до алкилбензолов и ацилируют (в присутствии катализатора AlCl3 хлорангидридами карбоновых кислот до жирноароматических кетонов (см. в статье реакция Фриделя – Крафтса). При алкилировании бензола этиленом образуется этилбензол, из которого в промышленности получают стирол; аналогично из бензола и пропилена образуется кумол – исходный продукт для получения фенола и ацетона. При окислении бензола кислородом воздуха при нагревании в присутствии катализатора получают малеиновый ангидрид. Бензол с трудом вступает в реакции присоединения. Так, только при фотохимическом хлорировании бензола образуется гексахлорциклогексан, используемый в качестве инсектицида. При каталитическом гидрировании бензол превращается в циклогексан – исходный продукт в производстве ε-капролактама.
Бензол содержится в коксовом газе, образующемся при пиролизе каменного угля. Основное количество бензола получают риформингом при 470–540 °C нефтяной фракции, выкипающей при 62–85 °C. Бензол – важнейшее сырьё химической промышленности, его применяют в производстве взрывчатых, душистых, лекарственных веществ, пестицидов, красителей, полимерных материалов, а также как растворитель и экстрагент в производстве лаков, красок и др.
Смеси бензола с воздухом (1,5–8 % бензола по объёму) взрывоопасны. Бензол токсичен, может вызывать острые и хронические отравления.