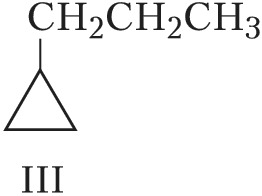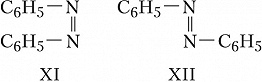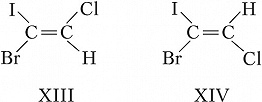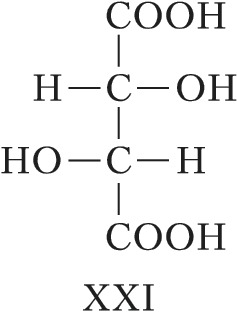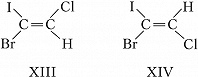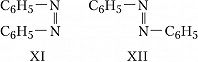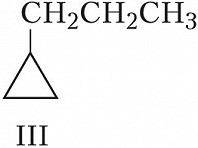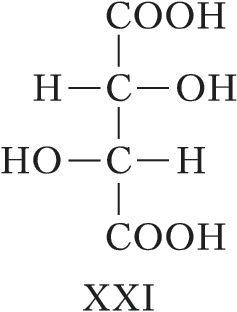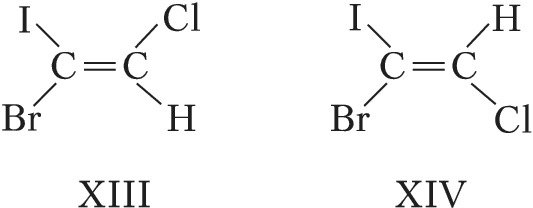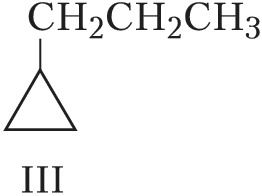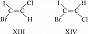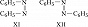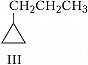ИЗОМЕРИ́Я
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
ИЗОМЕРИ́Я (от изо… и греч. μέρος – доля, часть), явление, заключающееся в существовании химич. соединений одинаковых по составу с одинаковой молекулярной массой, но различающихся по структуре. Такие соединения называются изомерами. Структурные различия обусловливают разл. взаимное влияние атомов в молекулах и предопределяют разные физич. и химич. свойства изомеров. И. чрезвычайно распространена в органич. химии и является одной из осн. причин разнообразия и многочисленности органич. соединений. В неорганич. химии И. встречается в осн. для комплексных соединений.
Термин «И.» ввёл Й. Берцелиус в 1830, завершая полемику между Ю. Либихом и Ф. Вёлером по вопросу существования двух резко отличающихся по свойствам веществ, имеющих один и тот же состав AgCNO, – цианата и фульмината серебра и опираясь на результаты исследований винной и виноградной кислот. Сущность И. была объяснена позднее на основе теории химич. строения.
Выделяют два осн. вида И.: структурную и пространственную (стереоизомерию). Структурные изомеры различаются порядком связей атомов в молекуле, т. е. химич. строением. Стереоизомеры (пространственные изомеры) при одинаковом порядке связей атомов в молекуле различаются взаимным расположением атомов в пространстве.
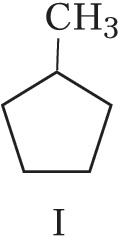
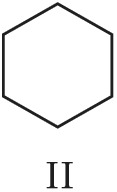
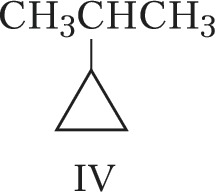
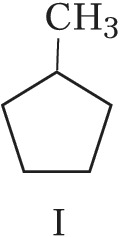
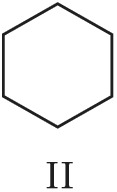
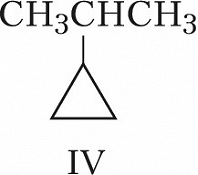
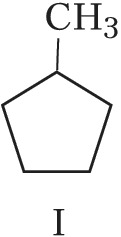
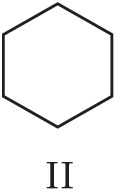
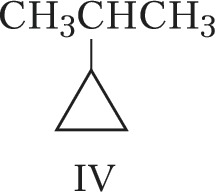
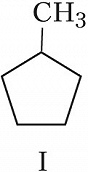
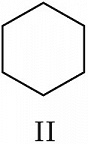
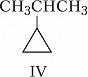
Структурная И. подразделяется на И. углеродного скелета (скелетную И.), И. положения (позиционную И.), метамерию и др. виды. И. углеродного скелета обусловлена разл. порядком связей углеродных атомов, образующих скелет молекулы. Для конкретизации структурных особенностей изомеров скелетная И. подразделяется на И. углеродной цепи, И. цикла и И. боковой цепи. Напр., И. углеродной цепи характерна для алканов начиная с четвёртого члена гомологического ряда $\ce{C_4 H_10}$, который имеет два структурных изомера: $\it н$-бутан $\ce{CH_3—CH_2—CH_2—CH_3}$ и изобутан (2-метилпропан) $\ce{CH_3—CH(CH_3)—CH_3}$. Пятый член ряда алканов $\ce{C_5H_{12}}$ имеет три изомера: $\ce{CH_3—CH_2—CH_2—CH_2—CH_3}$ – $\it н$-пентан, $\ce{CH_3—CH(CH_3)—CH_2—CH_3}$ – изопентан (2-метилбутан) и неопентан (2,2-диметилпропан) $\ce{CH_3—C(CH_3)_2—CH_3}$. С удлинением цепи число возможных изомеров быстро возрастает. Так, для алканов состава $\ce{C_{10}H_{22}}$ возможно существование 75 структурных изомеров, для $\cee{C_{13}H_{28}}$ – 802 изомеров, для $\ce{C_{20}H_{42}}$ – более 366 тыс. изомеров. Для алициклич. соединений характерны И. цикла и И. боковой цепи. Напр., среди скелетных изомеров (формулы I–IV) метилциклопентан (I), циклогексан (II) и пропилциклопропан (III) являются циклич. изомерами, а пропилциклопропан (III) и изопропилциклопропан (IV) – изомерами боковой цепи. Различия в свойствах скелетных изомеров проявляются в разнице их темп-р кипения (изомеры с нормальной углеродной цепью кипят при более высокой темп-ре, чем изомеры с разветвлённой цепью), плотности и др. $\it н$-Алканы, напр., в отличие от разветвлённых изомеров обладают меньшей детонационной стойкостью (см. в ст. Октановое число), образуют комплексы с мочевиной (клатраты).
И. положения обусловлена различным положением функциональных групп, заместителей или кратных связей. Например, изомерами положения являются 1-пропанол $\ce{CH_3—CH_2—CH_2OH}$ и 2-пропанол $\ce{CH_3—CH(OH)—CH_3}$, 1-бутен $\ce{CH_2=CH—CH_2—CH_3}$ и 2-бутен $\ce{CH_3—CH=CH—CH_3}$. Изменение положения функциональной группы может приводить к изменению класса соединения. Например, изомеры положения ацетон $\ce{CH_3—C(O)—CH_3}$ и пропаналь $\ce{CH_3—CH_2—CHO}$ относятся соответственно к кетонам и альдегидам. Структурные изомеры с разными функциональными группами сильно различаются по химич. свойствам.
Метамерия обусловлена разл. положением гетероатома ($\ce{O, N, S}$) в цепи. Напр., метамерами являются метилпропиловый эфир $\ce{CH_3—O—CH_2—CH_2—CH_3}$ и диэтиловый эфир $\ce{CH_3—CH_2—O—CH_2—CH_3}$, диэтиламин $\ce{CH_3—CH_2—NH—CH_2—CH_3}$ и $\ce{CH_3—NH—CH_2—CH_2—CH_3}$ – метилпропиламин.
Часто различия в изомерах определяют несколько структурных признаков. Например, метилизопропилкетон (3-метил-2-бутанон) $\ce{CH_3—C(O)—CH(CH_3)_2}$ и валериановый альдегид (пентаналь) $\ce{CH_3—CH_2—CH_2—CH_2—CHO}$ отличаются друг от друга как структурой углеродного скелета, так и положением функциональной группы.
Особым видом структурной И. является таутомерия (равновесная динамич. И.). В этом случае изомеры, различающиеся функциональными группами, легко переходят друг в друга до достижения равновесия, при котором вещество одновременно содержит молекулы таутомеров в определённом соотношении.
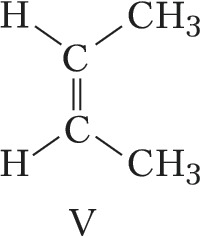
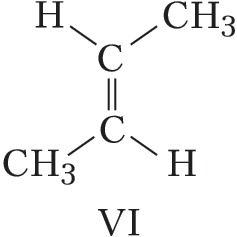
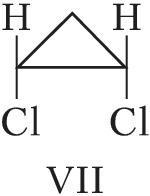
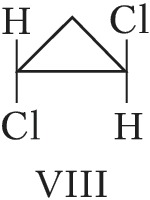
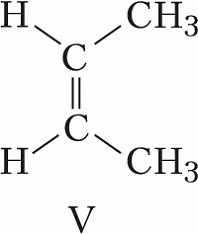
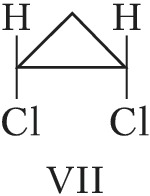
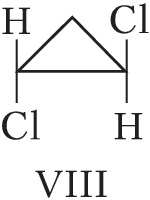
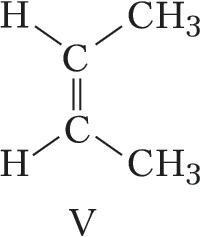
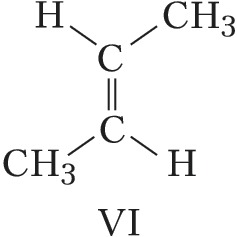
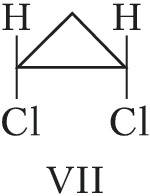
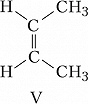
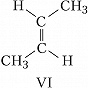
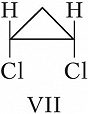
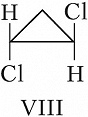
Пространственная изомерия подразделяется на геометрическую (цис,транс- и син,анти-изомерию, или $E,Z$-изомерию) и оптическую (энантиомерию). Геометрич. И. характерна для соединений, содержащих двойные связи или неароматич. циклы, являющиеся структурно жёсткими фрагментами молекул. У цис-изомеров два заместителя расположены по одну сторону плоскости двойной связи или цикла, у транс-изомеров – по разные стороны. Напр., геометрич. изомерами являются цис-2-бутен (формула V) и транс-2-бутен (VI), цис-1,2-дихлорциклопропан (VII) и транс-1,2-дихлорциклопропан (VIII).
Характерными различиями между цис- и транс-изомерами являются более низкая темп-ра плавления цис-изомеров, значительно лучшая растворимость в воде и явно выраженный дипольный момент. транс-Изомеры обычно более стабильны. См., напр., в ст. Малеиновая и фумаровая кислоты.
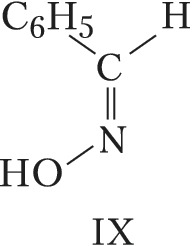
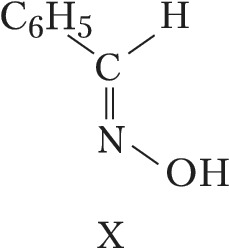
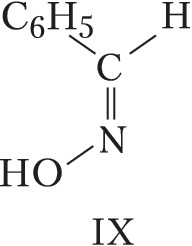
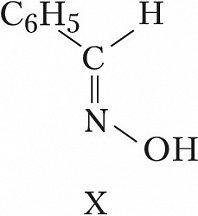
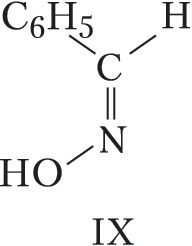
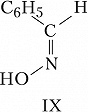
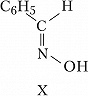
Геометрич. И., наблюдаемую для соединений с двойными связями $\ce{C=N}$ (оксимы) и $\ce{N=N}$ (азо-, азоксисоединения), часто называют син,анти-И. Напр., геометрич. изомерами являются анти-бензальдоксим (формула IX) и син-бензальдоксим (X); син-азобензол (XI) и анти-азобензол (XII).
В общем случае используется $E,Z$-номенклатура. У $Z$-изомеров старшие заместители (имеющие больший атомный номер) расположены по одну сторону двойной связи или цикла, у $E$-изомеров – по разные стороны. Напр., геометрическими изомерами являются ($Z$)-1-бром-1-иод-2-хлорэтилен (формула XIII) и ($E$)-1-бром-1-иод-2-хлорэтилен (XIV).
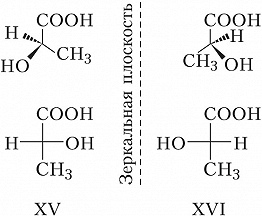
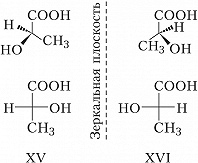
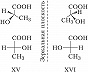
Оптич. И. характерна для соединений, молекулы которых имеют элементы хиральности, напр. асимметрич. (хиральный) атом углерода, связанный с четырьмя разными заместителями. Впервые обнаружена Л. Пастером в 1848 на примере винных кислот и объяснена Я. Х. Вант-Гоффом и Ж. А. Ле Белем в 1874 на основе представлений о тетраэдрич. конфигурации углеродных атомов в насыщенных соединениях. Молекулы, содержащие асимметрич. атом углерода, могут быть представлены в виде двух оптич. изомеров, которые не могут быть совмещены в пространстве (т. е. относятся друг к другу как предмет к своему зеркальному изображению). Такие зеркальные изомеры, отличающиеся лишь противоположным расположением одних и тех же заместителей у хирального центра, называются энантиомерами (от греч. ἐναντίος – противоположный и μέρος – часть). Напр., энантиомеры молочной кислоты (XV и XVI) можно представить в трёхмерном изображении или в виде формул Фишера (см. в ст. Химическая номенклатура).
Энантиомеры имеют разл. биологич. активность; для них характерна также оптич. активность – способность воздействовать на плоскополяризованный свет (вращать плоскость поляризации). Энантиомеры вращают плоскость поляризации на один и тот же угол, но в противоположном направлении, поэтому их называют оптич. антиподами.
Длительное время конфигурацию энантиомеров определяли относительно конфигурации известного стандарта, которым служили энантиомеры глицеринового альдегида (D, L-стерические ряды). Более универсальной является $R$, $S$-номенклатура (предложена Р. Каном, К. Ингольдом и В. Прелогом), устанавливающая абсолютную конфигурацию пространственных изомеров. В соответствии с правилами $R$, $S$-номенклатуры энантиомеры молочной кислоты (XV, XVI) являются соответственно ($R$)-молочной и ($S$)-молочной кислотами. Правил перевода D,L-номенклатуры в $R$, $S$-систему не существует, т. к. в этих номенклатурах используются разные принципы. Не установлено также связи между абсолютной конфигурацией и параметрами оптич. вращения.
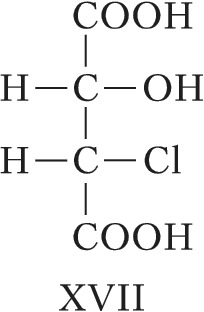
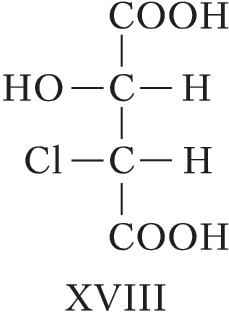
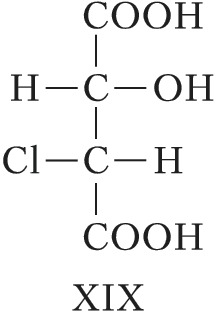
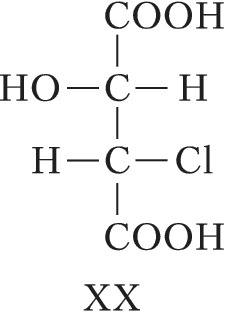
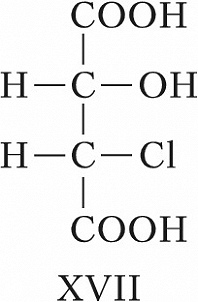
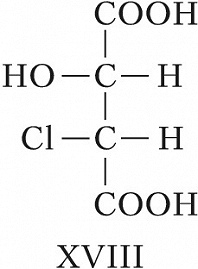
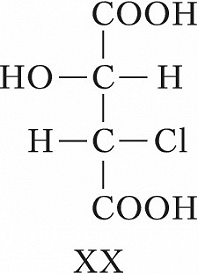
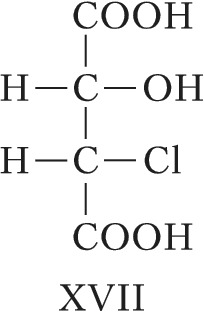
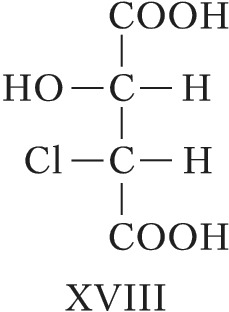
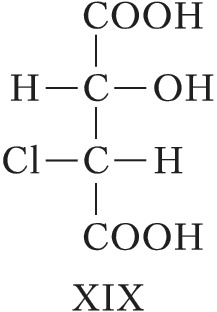
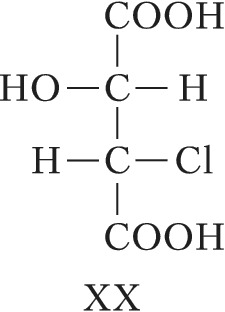
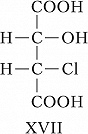
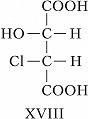
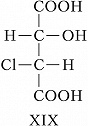
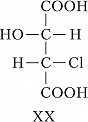
Для соединений, имеющих $n$ хиральных центров в молекуле, количество возможных стереоизомеров составляет $2^n$. Однако при $n⩾2$ существуют стереоизомеры, которые отличаются друг от друга частью имеющихся в них элементов хиральности. Такие стереоизомеры, не являющиеся энантиомерами, называют диастереомерами (от греч. δια... – через, между, стерео… и μέρος – часть). Напр., для хлоряблочной кислоты, имеющей два асимметрич. атома углерода, существуют четыре стереоизомера (формулы XVII–XX), среди которых пáры XVII и XVIII, а также XIX и XX являются энантиомерами, остальные пáры (XVII и XIX, XVII и XX, XVIII и XIX, XVIII и XX) – диастереомеры.
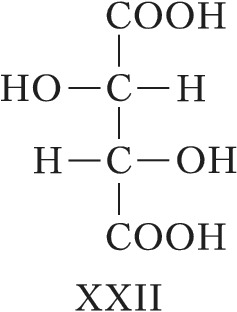
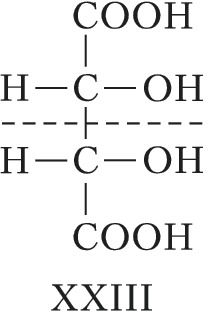
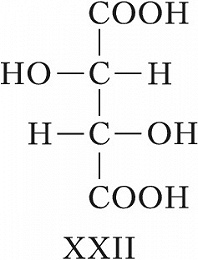
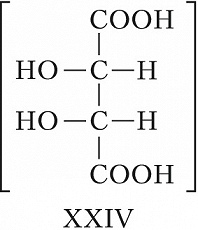
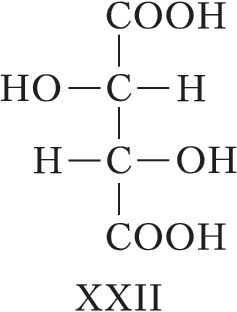
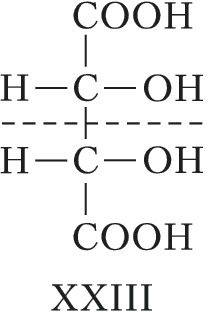
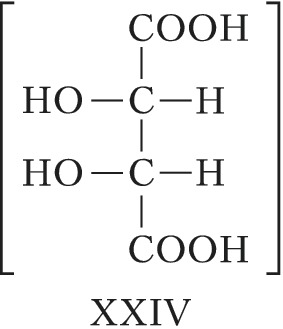
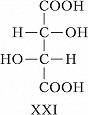
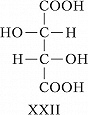
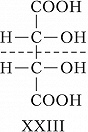
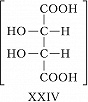
При появлении дополнит. элементов симметрии (плоскости, оси или центра симметрии) общее число стереоизомеров, а также количество оптически активных форм может уменьшаться. Напр., винные кислоты имеют три стереоизомера, из них два оптически активные: D-винная кислота, или ($2R,3R$)-винная кислота (формула XXI), и L-винная кислота, или ($2S,3S$)-винная кислота (XXII), являющиеся энантиомерами. Их диастереомер – мезовинная кислота, или ($2R,3S$)-винная кислота (формула XXIII, или идентичная конфигурация XXIV), вследствие наличия плоскости симметрии (обозначена пунктиром) оптически недеятельна – является т. н. внутримолекулярным рацематом.
Процесс взаимопревращения энантиомеров называется рацемизацией. Смесь равных количеств оптич. антиподов – рацемич. смесь, или рацемат, не обладает оптич. активностью. Стереоизомерии уделяется большое внимание при изучении природных соединений и синтезе биологически активных веществ. Веществам природного происхождения, содержащим элементы хиральности, присуща определённая стереоконфигурация, а также оптич. активность. При формировании хирального центра в условиях химич. синтеза (за исключением асимметрического синтеза) образуется рацемат; для выделения энантиомеров требуется применение сложных методов разделения рацемата на оптически активные компоненты.
В результате внутреннего вращения молекул возникают конформационные изомеры, или конформеры, различающиеся степенью поворота фрагментов молекулы относительно одной или нескольких простых связей. В некоторых случаях можно выделить отд. конформеры, иногда называемые также поворотными изомерами. Для изучения образования, различия в свойствах и реакционной способности конформеров используется конформационный анализ.
Изомеры могут превращаться друг в друга в результате реакций изомеризации.