ПОЛИМОРФИ́ЗМ
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
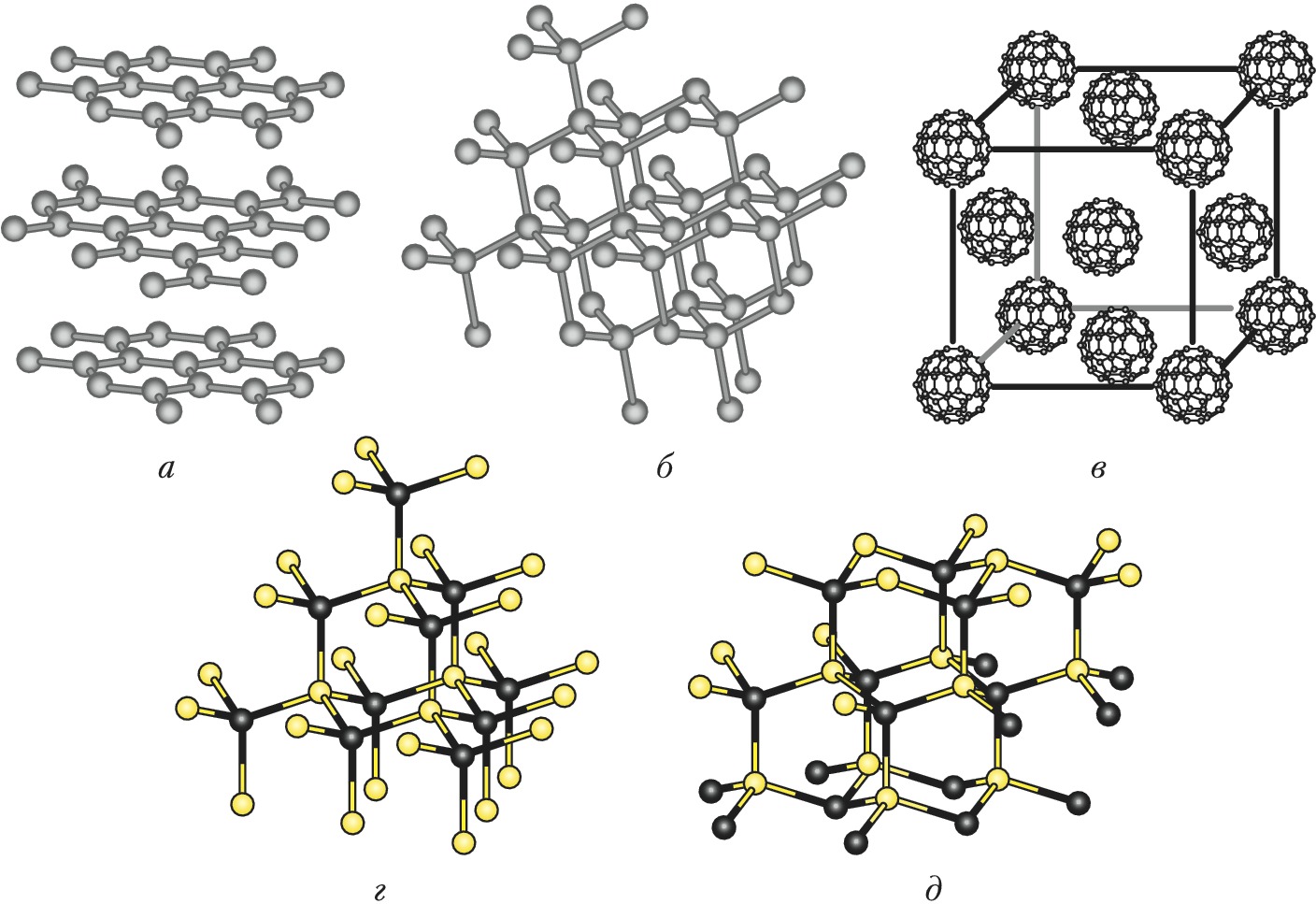
ПОЛИМОРФИ́ЗМ кристаллических веществ, способность соединений одинакового химич. состава существовать в двух или нескольких модификациях с различным расположением атомов или молекул в кристалле (кристаллической структурой). П. открыл М. Клапрот в 1798; термин «П.», введённый в 1822 Э. Митчерлихом, отражает различия в форме (огранке) кристаллов у разных полиморфных модификаций (полиморфов) вещества. Примерами полиморфных модификаций являются кристаллич. модификации углерода (алмаз, лонсдейлит, графит, фуллерены), ромбич. и моноклинная сера, минералы кальцит и арагонит состава CaCO3 и мн. др.
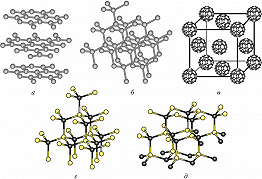
Различия кристаллич. структур полиморфных модификаций варьируются от глубокой перестройки (алмаз, графит, фуллерены; а, б и в на рис. 1) до изменений в связывании одинаковых фрагментов (минералы сфалерит и вюрцит состава ZnS; г и д на рис. 1) либо в их взаимной ориентации (молекулы S8 в полиморфных модификациях серы). Полиморфные модификации нередко различаются цветом и физико-химич. свойствами кристаллов: так, алмаз – твёрдый, бесцветный и прозрачный диэлектрик, графит – мягкий непрозрачный проводник серого цвета; составу HgS отвечают чёрный метациннабарит (изоструктурный сфалериту) и красная киноварь, построенная из бесконечных спиральных цепочек …─ S─ Hg─ S─ Hg─ S─ …, и т. д. П. простых веществ – частный случай аллотропии, охватывающей также некристаллич. формы (карбин и нанотрубки углерода, полимерная пластическая сера и др.). Полиморфные модификации, построенные из одинаковых двумерных атомных слоёв или слоевых пакетов, по-разному сдвинутых относительно друг друга, называются политипами (см. Политипия): в алмазе и лонсдейлите, а также в сфалерите и вюрците слои химически связаны; в политипах графита и др. слоистых кристаллов они соединены дисперсионными взаимодействиями.
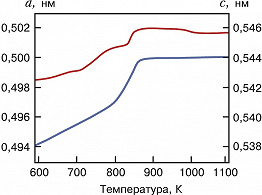
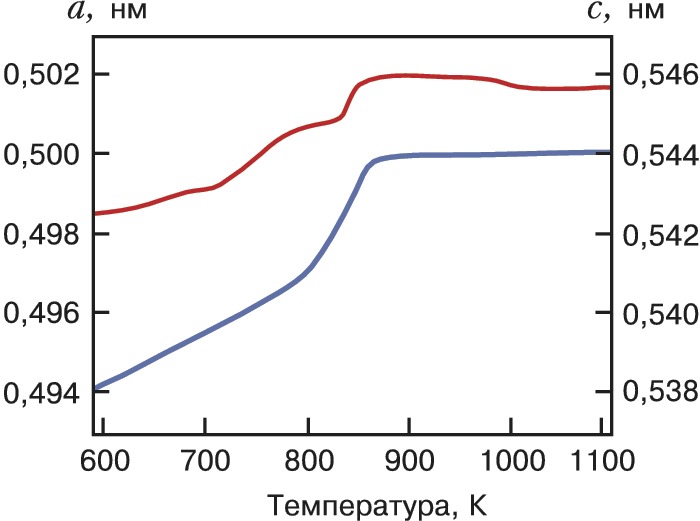
Разные полиморфные модификации заданного состава устойчивы при разных внешних условиях, прежде всего давлении (р) и темп-ре (Т). Полиморфные модификации часто обозначают строчными греч. буквами, обычно называя α-модификацией наиболее низкотемпературную. Фазовый переход 1-го рода из одной полиморфной модификации в другую (см. Структурные фазовые переходы) сопровождается резким скачком параметров элементарной ячейки кристалла (рис. 2) с изменением его симметрии и разрывом термодинамич. потенциалов в точке перехода. Переход между полиморфными модификациями с разной степенью упорядочения частиц (ферромагнитным α-Fe с одинаковой ориентацией магнитных моментов атомов и парамагнитным β-Fe, где они ориентированы произвольно при одной и той же кубич. объёмноцентрированной атомной структуре, низкотемпературной кристаллической и высокотемпературной ротационной фазами фуллерена С60, и т. д.), или переход «порядок – беспорядок», сопровождается быстрым изменением производных термодинамич. потенциалов (фазовый переход 2-го рода). Области устойчивости разл. полиморфных модификаций иллюстрируют фазовые диаграммы. Так, в интервале давлений 0–4 Мбар и температур 0–1000 К обнаружены 15 кристаллических и 3 аморфные модификации водных льдов Н2О (часть из них представлена на фазовой диаграмме в ст. Вода).
Прикладной аспект П. определяется различием свойств полиморфных модификаций. Напр., медленный переход тетрагонального белого олова (β-Sn) при темп-ре ниже 13 °С в изоструктурную алмазу кубическую α-форму меньшей плотности разрушает оловянные изделия («оловянная чума»). Огнеупорный кирпич на основе кремнезёма отжигают при темп-ре выше 1480 °С для перевода низкотемпературных полиморфных модификаций SiO2 (α- и β-кварц) в высокотемпературные (тридимит и кристобалит), чтобы избежать растрескивания при нагреве. Стабилизируя кубич. гранецентрированную структуру высокотемпературного γ-Fe при охлаждении образованием твёрдого раствора с 1–2% Ni или Mn (легирование) и углеродом, получают немагнитную аустенитную сталь. Особую важность П., очень характерный для органич. соединений, имеет в фармакохимии, т. к. полиморфные модификации лекарственных веществ различаются растворимостью, что влияет на их физиологич. активность.