АДИАБА́ТА
-
Рубрика: Физика
-
-
Скопировать библиографическую ссылку:
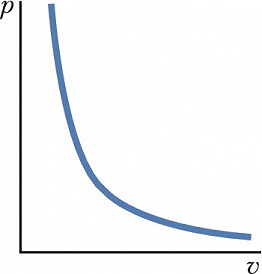
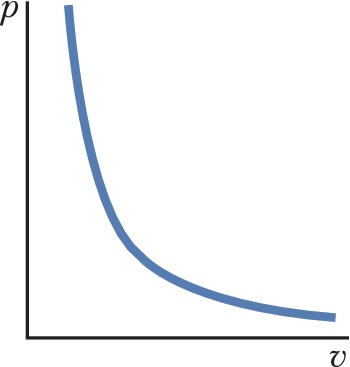
АДИАБА́ТА (от греч. ἀδιάβατος – непроходимый), линия на термодинамич. диаграмме состояния, изображающая равновесный адиабатический процесс. А. имеет простейший вид для идеальных газов с постоянной теплоёмкостью. Уравнение А. в этом случае: $pv^γ=const$, где $p$ – давление газа, $v$ – его удельный объём, $γ$ – показатель адиабаты, постоянная для данного газа величина, равная отношению теплоёмкостей газа, определённых при постоянном давлении $(c_p)$ и постоянном объёме $(c_v); γ=c_p/c_v$. Для одноатомных газов (аргона, неона и др.) при комнатной темп-ре $γ=1,67$, для двухатомных (водорода, азота, кислорода и др.) $γ=1,4$. На рис. изображена А. для $γ=1,4$. При очень низких темп-рах (вблизи абсолютного нуля) и при высоких (св. 1000 °С) характер кривой несколько иной, т. к. γ зависит от темп-ры и давления (см. Теплоёмкость).
Для равновесных (обратимых) адиабатич. процессов характерно постоянство энтропии, поэтому А. можно называть также изоэнтропой (изэнтропой).