АБСО́РБЦИЯ
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
АБСО́РБЦИЯ газов (лат. absorptio, от absorbeo – поглощать), объёмное поглощение газов и паров жидкостью или твёрдым телом (абсорбентами) с образованием раствора; частный случай сорбции. Процесс, обратный А., – десорбция. А. газов твёрдыми или расплавленными металлами с образованием твёрдых растворов или химич. соединений называется окклюзией. Различают физич. А., когда абсорбент является инертной средой по отношению к газу, и химич. А., когда поглощаемый компонент химически взаимодействует с абсорбентом (см. Хемосорбция).
Статика абсорбции
Характеризует термодинамич. равновесие раствора с парогазовой смесью, а также материальный и энергетич. балансы процесса. Количество абсорбированного газа зависит не только от природы газа и жидкости, но также от давления, темп-ры системы и состава газовой фазы. В состоянии равновесия концентрация поглощаемого вещества в газовой фазе $y^*$ связана с равновесной А. – концентрацией поглощаемого вещества в жидкой фазе $x^*$, равной растворимости данного газа в абсорбенте, соотношением: $y^*=mx^*$, где $m$ – константа фазового равновесия (коэф. распределения).
При физич. А. с образованием идеального раствора газа в абсорбенте, когда силы взаимодействия между всеми молекулами в растворе одинаковы, растворимость газа определяется законом Рауля, если газ способен конденсироваться при темп-ре раствора, или законом Генри – для газов, критич. темп-ра которых выше темп-ры раствора. Величину $m$ вычисляют исходя из термодинамич. свойств газа и жидкости или (чаще) определяют экспериментально. Поглотительная способность абсорбента – абсорбционная ёмкость, соответствующая предельному количеству газа, который поглощается единицей объёма абсорбента, и тепловой эффект процесса при химич. А. больше, чем при физической. При химич. А. растворимость сильно зависит от темп-ры. Влияние давления на ёмкость абсорбента обычно мало, поэтому химич. А. термодинамически более выгодна, особенно для извлечения из газовой смеси примеси при небольшой её концентрации.
Данные по равновесию газ–жидкость используют при определении константы фазового равновесия $m$, а также при расчёте движущей силы процесса, равной ($x^*_{гр}-x$) или ($y-y^*_{гр}$), где , – мольные доли жидкости и газа в объёме соответствующей фазы, $x^*_{гр}$, $y^*_{гр}$, – мольные доли жидкости и газа на межфазной поверхности. Отношение констант фазового равновесия для двух сравниваемых газов характеризует селективность абсорбента. Зависимость $y^*$ от при расчёте аппаратуры обычно называют равновесной линией.
Кинетика абсорбции
При А. поглощаемый газ в результате молекулярной, конвективной, а также турбулентной диффузии из ядра газового потока переносится к границе раздела фаз и по такому же механизму распределяется по объёму жидкости. Скорость переноса характеризуется массовым потоком $j$, т. е. числом молей вещества, переносимых за единицу времени через единицу площади межфазной поверхности по нормали к ней; $j=βx(x^*_{гр}-x)=βy(y-y^*_{гр})=K_y(y-y^*)$, где $β_x, β_y$ – коэффициенты массоотдачи для жидкой и газовой фаз, $K_y$ – коэф. массопередачи, отнесённый к газовой фазе, $y^*$ – мольная доля поглощаемого компонента в газе, которая отвечает равновесию с жидкостью состава $x$. Из уравнения $(1/K_y)=(1/β_y)+(m/β_x)$ определяют $m$ как тангенс угла наклона равновесной линии. При химич. А. скорость растворения газа в жидкости, как правило, выше, чем при физической. Этот эффект может быть выражен через увеличение движущей силы А. или (чаще) коэф. массоотдачи. Во втором случае используют т. н. коэф. ускорения $ϰ=β^ \prime_x/β_x$, где $β^\prime_x$ – коэф. массоотдачи в жидкой фазе при химич. А. Коэф. массоотдачи определяет скорость А. и позволяет рассчитать необходимую для заданной степени разделения (или очистки) газа высоту слоя насадки. Др. подход к расчёту кинетики процесса основан на предположении о достижении равновесия между жидкостью и газом в зоне контакта с последующим введением поправки, учитывающей эффективность ступени контакта (степень приближения к равновесию), равной отношению реализованного изменения состава к изменению, которое произошло бы при достижении равновесия.
При циклич. процессах физич. А. в осн. потребляется электроэнергия на перекачивание раствора, а при химич. А. – теплота на его регенерацию. Энергетич. затраты на регенерацию абсорбента обычно превышают расход энергии на А.
Основы технологии абсорбционных процессов
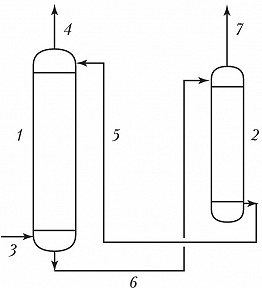
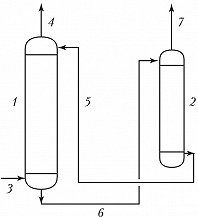
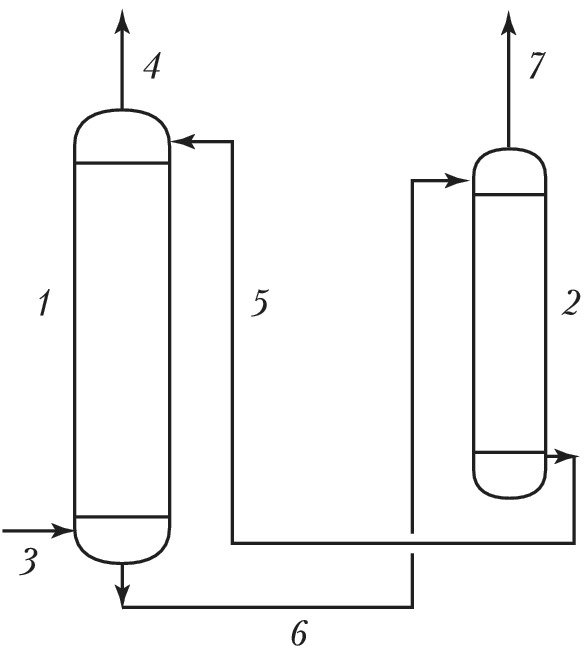
В пром-сти процесс А. осуществляют обычно в вертикальных колонных аппаратах – абсорберах, имеющих развитую поверхность соприкосновения газа и жидкости. Наиболее распространены насадочные аппараты (устар. – скрубберы), заполненные слоями твёрдых тел разл. размеров и формы – насадками для создания развитой поверхности контакта фаз, и тарельчатые аппараты, снабжённые расположенными одна над другой поперечными перегородками разл. конструкции, или тарелками, с помощью которых по высоте колонны осуществляется многократный дискретный контакт газа (пара) с жидкостью. Процесс часто осуществляют по абсорбционно-десорбционному циклу (см. рис.), однако стадия десорбции может отсутствовать, если в результате А. получают готовый продукт или регенерация поглотителя нецелесообразна (невозможна). Регенерацию абсорбента (десорбцию газов) можно проводить снижением давления, нагреванием, отдувкой плохо растворимыми газами и парами кипящего абсорбента.
Физич. А., как правило, наиболее эффективна при грубой очистке от больших количеств газа под давлением. Химич. А. чаще всего применяют при извлечении малых количеств примесей и при тонкой очистке; при этом обычно существенно выше селективность абсорбента, ниже количество циркулирующего раствора вследствие большой поглотительной способности.
Абсорбция в природе и технологии
А. широко распространена в природе: процессы А. определяют содержание кислорода в реках и озёрах, поверхностных слоях морей и океанов, регулируют физиологич. процессы в живых организмах и пр. Наиболее распространённые области практич. применения процессов А.: многотоннажные произ-ва серной, соляной и азотной кислот, нитратов и др. солей; выделение ценных компонентов из газовых смесей – бензина из коксового газа, ацетилена из газов крекинга или пиролиза природного горючего газа, бутадиена из контактного газа после разложения этилового спирта и пр.; очистка газа от примесей вредных компонентов – нефтяных и коксовых газов от $\ce{H2S}$, азотоводородной смеси для синтеза аммиака от СО2 и СО, санитарная очистка газов, выпускаемых в атмосферу, – топочных газов ТЭЦ от SO2, абгаза от Cl2, рекуперация летучих растворителей и др.