Ониевые соединения
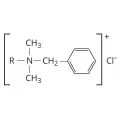
О́ниевые соедине́ния, соединения общей формулы Rn+1M+X–, где R – атом водорода, алкил (Alk), арил (Ar) или другой органический радикал; M – т. н. ониевый атом N, P, O, S, галоген и др. (соответственно аммониевые R4N+X–, фосфониевые R4P+X–, оксониевые R3O+X–, сульфониевые R3S+X–, галогенониевые R2Hal+X– и другие соединения), n – низшая степень окисления M в органических соединениях, X – анион (Cl–, Br–, I–, OH–, BF4–, HSO4– и др.). Положительно заряженный ониевый атом связан ковалентной связью с органическими радикалами и водородом, образуя ониевый катион, который связан ионной связью с анионом. Замещение в ониевых катионах, не содержащих органических радикалов, таких как катион аммония H4N+, фосфония H4P+, оксония H3O+, сульфония H3S+ и т. д., атомов водорода на органические радикалы приводит к первичным (например, алкиламмоний [RNH3]+), вторичным (диалкиламмоний [R2NH2]+), третичным (триалкиламмоний [R3NH]+) или четвертичным (тетраалкиламмоний [R4N]+) ониевым катионам. Ониевый атом может входить в состав гетероцикла (пример – соли пирилия) или какой-либо группы (например, в случае катиона нитрилия [RC≡NR]+).
Ониевые соединения – кристаллические солеобразные вещества, растворяются в полярных органических растворителях и в воде; водные растворы обладают высокой электропроводностью. Стабильность ониевых соединений зависит от природы ониевого атома, аниона, органического радикала; так, алифатические оксониевые соединения устойчивы только с комплексными анионами (например, BF4–) в отсутствие влаги. Гидроксиды ониевых соединений (X−OH) – сильные основания, превращающиеся при нагревании в олефины (в случае M – N, S, Se) или алканы (M – P, As, Sb). Алифатические ониевые соединения обычно получают алкилированием алкилгалогенидами или алкилтозилатами алкилпроизводных, содержащих на один алкильный остаток меньше, чем синтезируемое ониевое соединение: (X – галоген, 4-CH3C6H4SO2); ароматические – термолизом арилдиазонийтетрафторборатов в среде арилпроизводных, содержащих на один арильный остаток меньше, чем синтезируемое ониевое соединение: .
Многие ониевые соединения обладают физиологической активностью. Ониевые структуры входят в состав природных и биологически важных соединений (бетаины, холин и др.). Ониевые соединения являются промежуточными продуктами, алкилирующими или арилирующими реагентами во многих органических реакциях, используются в производстве красителей, в качестве нейтральных поверхностно-активных веществ, катализаторов, стабилизаторов, эмульгаторов, инсектицидов, гербицидов и др.