НИТРОСОЕДИНЕ́НИЯ
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
НИТРОСОЕДИНЕ́НИЯ, органич. соединения, содержащие нитрогруппу NO2, непосредственно связанную с атомом углерода. Изомерны эфирам азотистой кислоты (органическим нитритам). Соединения с нитрогруппой при атоме азота и кислорода выделяют в отд. классы (соответственно нитрамины и органические нитраты).
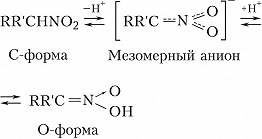
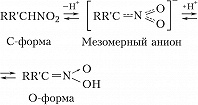
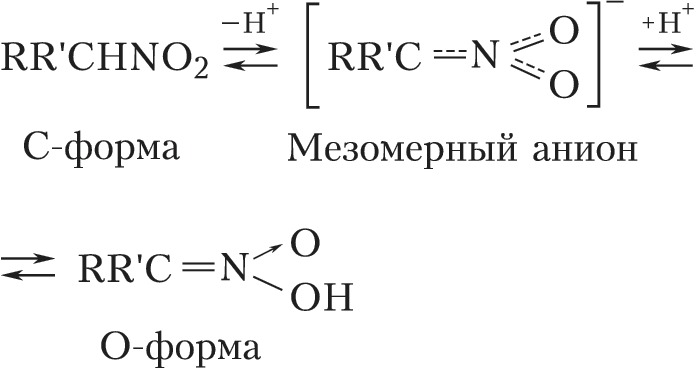
По числу нитрогрупп различают моно-, ди- и полинитросоединения; по положению – алифатические (нитроалканы и нитроалкены), ароматические (напр., нитробензол, нитротолуолы, нитронафталины), жирноароматические (напр., нитростирол C6H5CH═CHNO2) и смешанные (напр., п-нитрофенилнитрометан O2NC6H4CH2NO2) Н. Ароматич. Н. относятся к третичным, остальные Н. могут быть первичными, вторичными и третичными. Н., имеющие в α-положении атом водорода, могут существовать в двух таутомерных формах:
Кислотная O-форма Н. называется аци-формой или нитроновой кислотой. Мн. превращения алифатич. Н. проходят с предварит. изомеризацией в нитроновые кислоты или с образованием мезомерного аниона. В растворах равновесие обычно практически полностью сдвинуто в сторону С-формы. Нитроновые кислоты в свободном виде неустойчивы, известны их производные (соли, эфиры и т. д.).
Простейшие алифатич. Н. – бесцветные жидкости; ароматич. Н. – бесцветные или светло-жёлтые высококипящие жидкости или низкоплавкие твёрдые вещества, обладающие характерным запахом (напр., запах горького миндаля у нитробензола). Н. плохо растворяются в воде, хорошо – во многих органич. растворителях. Алифатич. Н. хорошо растворяют разл. органич. соединения. При нагревании большинство Н. разлагается (часто со взрывом).
Реакционная способность Н. обусловливается как склонностью нитрогруппы к разл. превращениям, так и влиянием её на др. реакционные центры в молекуле. Введение группы NO2 – сильнейшего электроноакцепторного заместителя, способного эффективно делокализовать отрицательный заряд, резко увеличивает реакционную способность органич. соединений по отношению к нуклеофильным реагентам и затрудняет реакции с электрофильными реагентами.
Алифатич. Н. восстанавливаются до гидроксиламинов и аминов, образуют соли при действии оснований. Для них характерны реакции по подвижному атому водорода, в т. ч.: присоединение в присутствии оснований к альдегидам и кетонам с образованием нитроспиртов (реакции Анри); присоединение к соединениям, содержащим активированную двойную связь (реакция Михаэля); взаимодействие с алифатич. аминами и СН2О с образованием β-аминопроизводных (реакция Манниха); галогенирование, алкилирование, ацилирование. Анионы алифатич. Н. реагируют с электрофилами по двум направлениям: [RR′CNO2]–M++Eδ+─Nuδ–→ RR′C(NO2)E+ RR′C N(O)OE+ M+Nu– (M+ – катион металла, NH4; E – алкил, ацил, R3Si, RS и др.; Nu – галоген, SO3R и др.). Под действием сильных кислот происходит перегруппировка алифатич. Н. до гидроксамовых кислот, которые затем легко гидролизуются; метод используют в пром-cти для синтеза СН3СООН и гидроксиламина из нитроэтана.
Ароматич. Н. восстанавливаются до аминов (важное свойство ароматич. Н. – их способность давать ряд продуктов восстановления; напр., нитробензол последовательно восстанавливается до нитрозобензола, N-фенилгидроксиламина, азоксибензола, азобензола, гидразобензола, аминобензола – анилина); образуют аддукты с ароматич. углеводородами, аминами, щелочами и др.; нитрогруппа и атомы водорода цикла способны замещаться на др. функциональные группы. Реакции нуклеофильного замещения происходят легко, электрофильного – затруднённо; нуклеофил направляется в орто- и пара-положения, электрофил – в мета-положения к группе NO2. Активирующее влияние группы NO2 на нуклеофильное замещение широко используют в органич. синтезе.
В пром-сти ароматич. Н. получают нитрованием ароматич. соединений смесью серной и азотной кислот, а также окислением нитрозо-, диазо- и аминоаренов; алифатич. Н. – гл. обр. жидкофазным нитрованием алканов (реакция Коновалова) азотной кислотой или оксидами азота. Для получения низших нитроалканов используют также парофазное нитрование смеси этана, пропана и бутана, выделяемых из природного газа или полученных переработкой нефти.
Поли-Н., особенно ароматические, применяют в качестве взрывчатых веществ (напр., тринитрофенол, тринитротолуол). Алифатич. Н. используют как растворители в лакокрасочной и полимерной пром-сти; для очистки минер. масел; депарафинизации нефти и др. Восстановлением ароматич. Н. получают ароматич. амины – полупродукты в произ-ве разл. красителей. Ряд Н. находят применение в качестве инсектицидов, фунгицидов, гербицидов и антибиотиков. Некоторые ароматич. Н. – душистые вещества. Н. – реагенты в органич. синтезе, полупродукты в произ-ве полимеров, пластификаторов и модификаторов полимеров, ингибиторов коррозии, смачивающих, эмульгирующих и диспергирующих агентов.
Н. токсичны, могут оказывать наркотич. действие, вызывать поражение печени, почек, иногда глаз (катаракта), нарушать функции нервной системы, вызывать раздражение дыхат. путей, кожи и слизистых оболочек; ароматич. Н. – метгемоглобинемию.