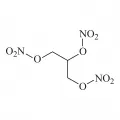
Нитроглицерин
Нитроглицери́н (глицеринтринитрат), полный эфир глицерина и азотной кислоты, O2NOCH2CH(ONO2)CH2ONO2.
Историческая справка
Впервые синтезирован итальянским химиком А. Собреро в 1847 г.; техническое использование предложено А. Б. Нобелем, организовавшим промышленное производство в 1860–1870-х гг.
Физико-химические свойства
Нитроглицерин – бесцветная маслянистая жидкость, склонная к переохлаждению и стеклованию; молярная масса 227,14 г/моль; кристаллизуется в лабильной (tпл 2,8 °C) и стабильной (tпл 13,5 °C) модификациях; плотность 1,593 г/см3 (при 25 °C). Растворяется в ацетоне, диэтиловом эфире, метаноле, бензоле, нитробензоле, плохо растворяется в воде; является хорошим растворителем нитросоединений (в частности, пластифицирует нитроцеллюлозу). Нитроглицерин взрывоопасен; взрывается при очень слабом механическом воздействии (ударе, трении). Горение нитроглицерина легко переходит во взрыв. Теплота взрыва 6,2 МДж/кг, скорость детонации около 7,7 км/с, температура вспышки около 200 °C.
По химическим свойствам нитроглицерин – типичный представитель органических нитратов. Медленно гидролизуется в воде, быстро – в кислотах; легко омыляется щелочами. При нагревании выше 50 °C происходит разложение нитроглицерина, сопровождаемое окислением и гидролизом; при 150 °C изотермическое разложение резко самоускоряется в результате накопления продуктов распада, что может привести к саморазогреву и взрыву.
В больших концентрациях нитроглицерин токсичен; может всасываться в кровь через кожу и вызывать головную боль.
Получение
Получают нитроглицерин этерификацией глицерина смесью (1:1) серной и азотной кислот. Поскольку нитроглицерин является одним из наиболее опасных в обращении взрывчатых веществ, его не хранят и не транспортируют, а сразу перерабатывают.
Применение
Hитроглицерин – мощное бризантное взрывчатое вещество, используется как компонент динамитов и порохов. Нитроглицерин оказывает сосудорасширяющее действие, в медицинской практике применяется в виде разбавленного спиртового раствора (в каплях) и в таблетках для купирования приступов стенокардии.