АЗЕОТРО́ПНЫЕ СМЕ́СИ
-
Рубрика: Химия
-
-
Скопировать библиографическую ссылку:
АЗЕОТРО́ПНЫЕ СМЕ́СИ, азеотропы (от a..., греч. ζέω – кипеть и τροπῄ – поворот, изменение), нераздельнокипящие жидкие растворы, т. е. растворы, для которых при данной темп-ре, давлении и концентрации компонентов составы равновесных фаз (жидкости и пара) одинаковы. А. с. могут быть двух- или многокомпонентными. Существование двухкомпонентных А. с. открыто в 1810 Дж. Дальтоном, который обнаружил, что в конце перегонки водных растворов соляной или азотной кислот темп-ра кипения и состав дистиллята остаются неизменными. Ок. 50% жидких смесей образуют азеотропы.
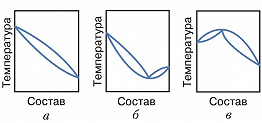
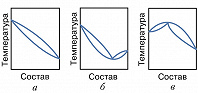
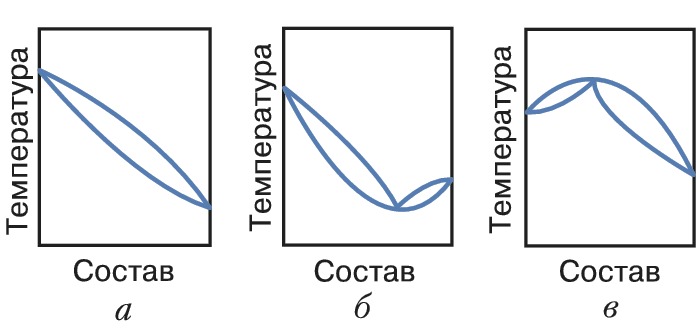
А. с., состоящие из одной жидкой фазы, называются гомоазеотропными, из двух или более – гетероазеотропными. А. с. могут быть положительными и отрицательными. Положит. А. с. на диаграмме фазового равновесия при постоянной темп-ре в азеотропной точке имеют максимум, при постоянном давлении – минимум; отрицат. А. с. обладают обратными свойствами (рис.). Среди бинарных растворов отрицат. азеотропы составляют менее 10% от общего числа известных А. с. Составы А. с. изменяются с темп-рой (давлением). Эта зависимость на фазовой диаграмме образует линию азеотропов, которая может проходить через всю область существования равновесия жидкость–пар, вплоть до критич. кривой. Вдали от критич. кривой положение азеотропной точки будет изменяться тем в большей степени, чем сильнее различаются парциальные молярные теплоты испарения компонентов (см. Вревского законы). Возможно состояние, когда азеотропная точка сместится за край фазовой диаграммы и А. с. станет зеотропной – раздельнокипящей.
Азеотропная точка может соответствовать очень малым концентрациям одного из компонентов; напр., в системе гексан–бензол азеотропная точка расположена в интервале концентраций 99,781–99,796 мол. % гексана. В осн. известны двухкомпонентные А. с. с одной азеотропной точкой. В системе бензол–гексафторбензол экспериментально обнаружены две азеотропные точки. Бесконечное множество азеотропных точек возможно в системах изотопнозамещённых молекул, напр. в системе вода–тяжёлая вода.
Термины «положительные» и «отрицательные» А. с. связаны с положит. и отрицат. отклонениями свойств жидких смесей от поведения идеальных растворов. Добавление к двойной неидеальной системе третьего компонента может увеличить или уменьшить её неидеальность. Поэтому тройной азеотроп может появиться в соответствующих зеотропных двойных системах и, наоборот, тройная система может быть зеотропной при наличии азеотропов в образующих её двойных системах.
Для разделения А. с. используют азеотропную ректификацию (напр., абсолютный этиловый спирт получают азеотропной ректификацией с разделяющим агентом – бензолом), ректификацию в условиях, когда растворы зеотропны во всём интервале концентраций (напр., водно-спиртовые растворы разделяют при давлении ниже 70 мм рт. ст.), а также методы, не связанные с равновесием жидкость–пар. Изучение А. с. обусловлено необходимостью разделения пром. смесей на индивидуальные компоненты.